기본원리 (The principle)
기체의 압력을 P, 부피를 V, 섭씨온도를 t, 절대온도를 T라고 하자.
Let's denote the pressure of the gas as P, the volume as V, the temperature in Celsius as t and the absolute temperature as T.
온도가 일정한 상황에 기체에 압력을 가하면 부피가 줄어든다.
즉, 기체의 부피는 압력에 반비례하며 이를 '보일의 법칙'이라고 한다.
In a situation where the temperature is constant, if pressure is applied to a gas, its volume decreases. In other words, the volume of the gas is inversely proportional to the pressure, and this relationship is known as 'Boyle's Law'.
PV = k (일정, constant)
압력이 일정한 상황에서 기체에 열을 가하면 부피가 늘어난다.
기체의 온도가 1 ℃ 상승할 때마다 기체가 0 ℃일 때의 부피의 1/273씩 부피가 팽창하는데, 이를 식과 그래프로 나타내면 아래와 같다.
In a situation where pressure is constant, if heat is applied to a gas, its volume increases.
Specifically, for each 1 ℃ increase in temperature, the volume of the gas at 0 ℃ expands by 1/273 of its original volume. This relationship can be expressed with the following equation and graph:
Vt = Vo (1 + t/273)
Vt : 나중 부피, final volume
Vo : 처음 부피, initial volume
t : 섭씨온도, temperature in Celsius
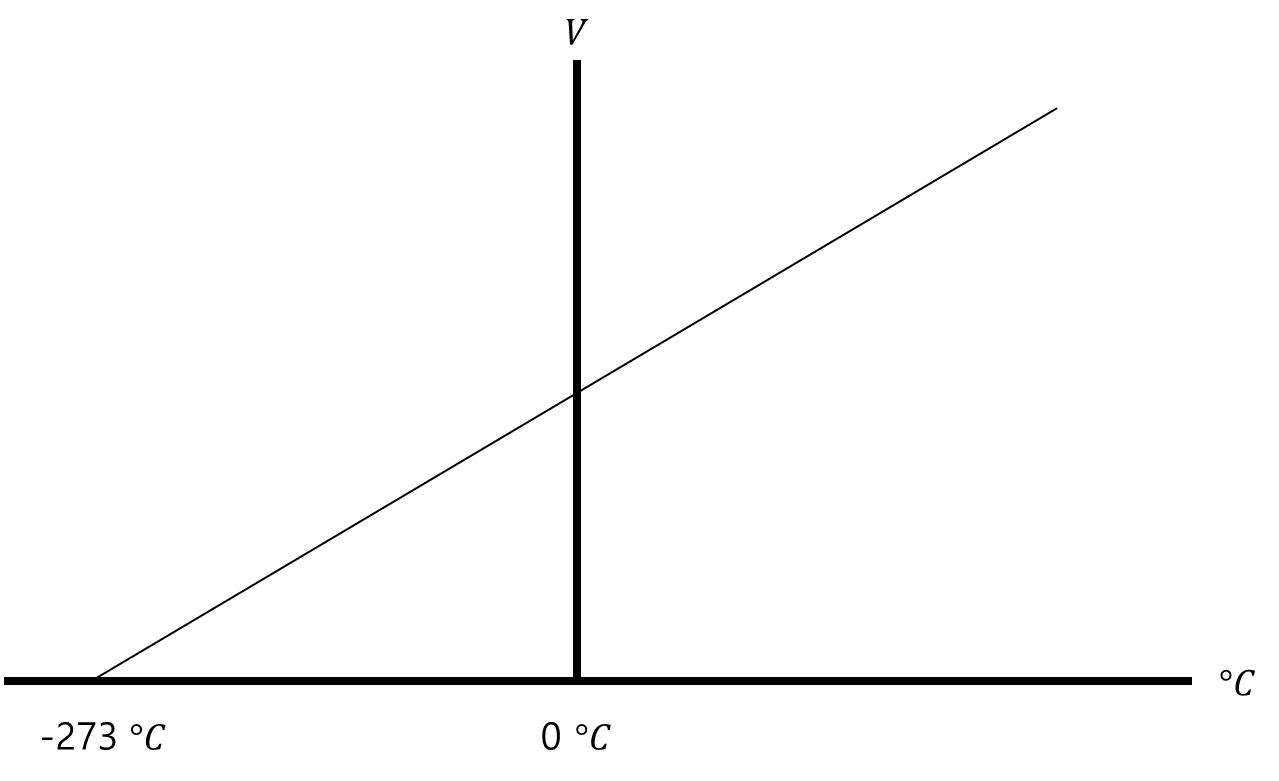
위 식에 의하면, 기체의 온도가 1 ℃ 감소하면 기체의 부피는 0 ℃일 때 부피의 1 / 273씩 줄어들어 기체의 온도가 - 273 ℃가 되면 기체의 부피는 0이 된다.
기체의 부피가 0이 되는 온도인 - 273 ℃를 '절대영도'라고 하며, 섭씨온도에 273을 더하여 '절대온도'라고 한다.
절대온도인 T(단위: K)를 이용하면 아래와 같이 식과 그래프를 나타낼 수 있으며 이를 '샤를의 법칙'이라고 한다.
According to the equation, when the temperature of a gas decreases by 1 ℃, the volume of the gas decreases by 1/273 of its volume at 0 ℃. If the gas's temperature reaches -273 ℃, the volume becomes 0.
The temperature at which the volume of a gas becomes 0, -273 ℃, is known as 'absolute zero.' To convert from Celsius to absolute temperature, 273 is added. This absolute temperature is represented as T (unit: K). Using absolute temperature, the equation and graph can be expressed as follows, which is known as 'Charles's Law.'
V / T = k (일정, constant)

보일의 법칙과 샤를의 법칙을 하나의 공식으로 나타내면 다음과 같다.
이 공식에 의하면, 온도가 일정할 때 부피는 압력에 반비례하며 압력이 일정할 때 온도는 부피에 비례한다.
The combined law representing Boyle's law and Charles's law is expressed as follows:
According to this formula, when the temperature is constant, volume is inversely proportional to pressure, and when pressure is constant, volume is directly proportional to temperature.
PV / T = k (일정, constant)
문제풀이 (Problem solving)
Q: 최고사용압력이 5 kg/cm²g인 용기에 20 ℃, 2 kg/cm²g인 가스가 채워져 있다. 이 가스의 온도는 몇 ℃까지 상승하는가?
Q: A vessel with a maximum allowable pressure of 5 kg/cm²g is filled with gas at 20 °C and 2 kg/cm²g. By how many degrees Celsius can the temperature of this gas increase?
A: 20 ℃, 2 kg/cm²g인 가스의 압력은 최고사용압력인 5 kg / cm2g까지 상승할 수 있다.
이 때의 온도를 알기 위해서, 위에서 유도한 식을 이용하여 문제에 주어진 압력 값을 대입하면 다음과 같다.
여기서 주의할 점은 T가 절대온도라는 것이다.
A: The gas, with an initial pressure of 2 kg/cm²g at 20°C, can increase its pressure to the maximum allowable pressure of 5 kg/cm²g. To find the corresponding temperature, we can use the derived equation by substituting the given pressure values into it.
It's important to note that T represents the absolute temperature in this context.
(5 kg/cm²g) V / (t + 273) = (2 kg/cm²g) V / (20 ℃ + 273) = k (일정, constant)
5 V / (t + 273) = 2 V / 293
5 / 2 = (t + 273) / 293
2.5 X 293 = t + 273
t = 459.5 ℃
즉, 가스의 온도는 459.5 ℃까지 상승할 수 있다.
In other words, the temperature of the gas can increase up to 459.5°C.
'화학 문제 풀이 (Chemistry)' 카테고리의 다른 글
| 전기 화학, 석출 속도 (2) | 2023.10.28 |
|---|---|
| 고려청자 비취색의 비밀 (0) | 2023.10.22 |
| 화학반응으로 생성된 화학물질의 양 (Quantity of chemical substance produced by a chemical reaction) (2) | 2023.10.21 |
| 침전되는 AgCl의 질량 (The mass of precipitated AgCl) (0) | 2023.10.16 |
